Soru 1 |
Metal malzeme satan bir işletmenin sahibi her biri 5,4 kg olan bir miktar demir malzemesi almış ancak 3 ay boyunca satamamıştır. Malzeme listesini kütlelerini de hesaba katarak güncelleyen işletme sahibi 3 aydır dükkanının nemli bölgesinde bulunan demir malzemesinin her birinin kütlesini 6 kg olarak ölçmüştür.
Buna göre,
I. Demir malzemeler havanın oksijeni ile 4Fe(k) + 3O2 (g) → 2Fe2O3 (k) tepkimesine girmiş olabilir.
II. Kütlesi artan her bir demir malzeme havanın 600 gram oksijeni ile tepkimeye girmiştir.
III. Ortamdaki toplam kütle artmıştır.
yargılarından hangilerine ulaşılabilir?
Yalnız I. | |
Yalnız II. | |
Yalnız III. | |
I ve II. | |
I ve III. |
Soru 2 |
Bir bileşiği oluşturan elementlerin kütleleri arasında her zaman sabit bir oran vardır. Bileşiğin miktarı değişse de bileşiği oluşturan elementlerin kütlece birleşme oranı değişmez.
Tabloda X ve Y elementlerinden oluşan iki farklı bileşiğe ait bilgiler verilmiştir.

Buna göre,
I. Aynı iki elementten oluşan bütün bileşiklerin kütlece birleşme oranları da aynıdır.
II. 1. bileşiği oluşturan elementlerin harcanan kütleleri arasındaki oran ![]()
III. 2. bileşiği oluşturan elementlerden eşit kütlelerde alınarak tam verimle bir tepkime gerçekleştiğinde artan madde olmaz.
ifadelerinden hangileri doğrudur?
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 3 |
Aynı iki element basit formülleri farklı birden fazla bileşik oluşturuyorsa, bu elementlerden birinin eşit miktarı ile birleşen diğer elementin miktarları arasında tam sayılarla ifade edilen katlı bir oran vardır.
Buna göre,
I. Soru:
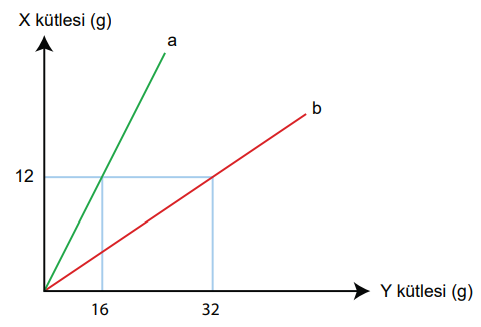
X ve Y elementlerinden oluşan a ve b bileşiklerinin kütle değişim grafiğine göre a bileşiğinin formülü XY ise, b bileşiğinin formülü nedir?
II. Soru:
a bileşiği: Fe2O3 b bileşiği: Fe3On
a ve b bileşiklerinde, eşit miktarda Fe elementi ile birleşen a bileşiğindeki O elementinin b bileşiğindeki O elementine oranı ![]() olduğuna göre “n” değeri kaçtır?
olduğuna göre “n” değeri kaçtır?
II. Soru:
Eşit kütlelerde X ve Y elementleri alınarak başlatılan tepkime tam verimle gerçekleşiyor ve 17 gram XY2 bileşiği oluşurken 3 gram X elementinden artıyor. Buna göre başlangıçta X ve Y elementlerinden kaçar gram alınmıştır?
sorularından hangileri katlı oranlar kanunundan yararlanılarak çözülebilir?
Yalnız I. | |
Yalnız II. | |
I ve II. | |
II ve III. | |
I, II ve III. |
Soru 4 |
Mol kavramı, günlük hayatta kullanılan deste ve düzine gibi maddelerin sayısını ifade etmeye yarayan bir kavramdır ve 1 deste 10, 1 düzine 12, 1 mol 6,02.1023 sayısına karşılık gelir.
Buna göre,
I. 3,01.1022 tane C atomu, 0,5 mol C atomudur.
II. 6,02.1023 tane Ag atomu, 1 mol Ag atomudur.
III. 2 mol Mg atomu, 1,204.1024 tane Mg atomudur.
yargılarından hangileri doğrudur?
Yalnız I. | |
Yalnız II. | |
I ve II. | |
II ve III. | |
I, II ve III. |
Soru 5 |
Kimyanın temel kanunları ile ilgili;
1. Kimyasal tepkimelerde tepkimeye giren maddelerin kütleleri toplamı, tepkime sonucunda oluşan maddelerin kütleleri toplamına eşittir.
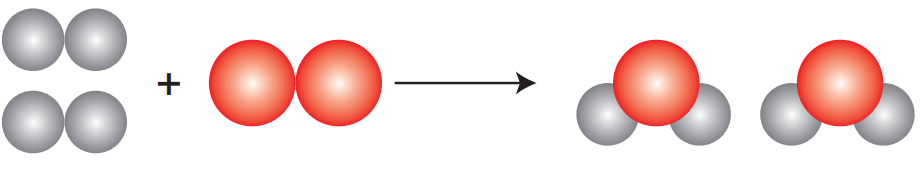
2. Bir bileşiği oluşturan elementlerin kütleleri arasında sabit bir oran vardır.
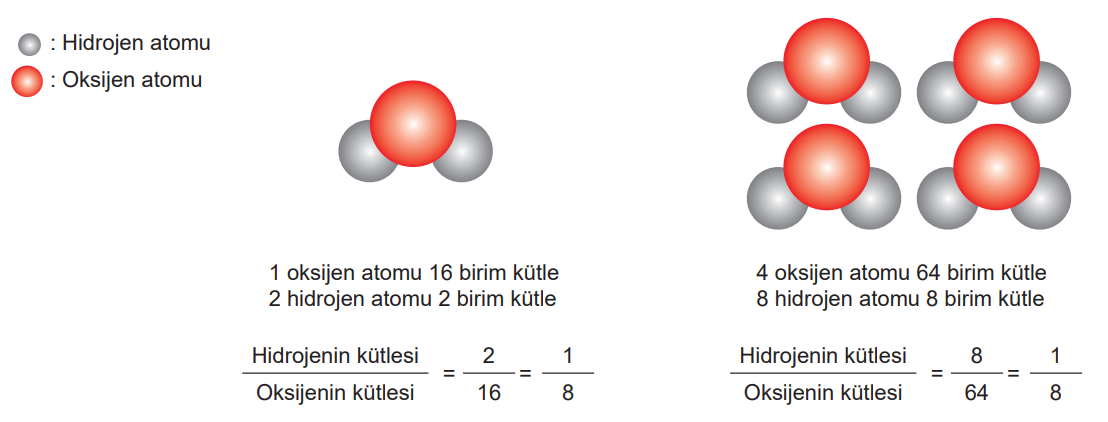
3. İki element birden fazla bileşik oluşturmak için bir araya geldiğinde bir elementin belirli bir kütlesiyle birleşen diğer elementin kütleleri arasında basit bir oran vardır.
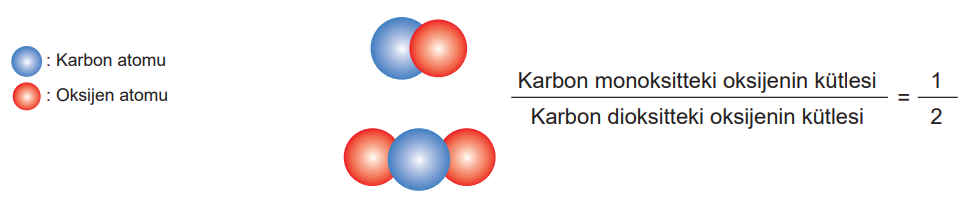
bilgileri veriliyor.
Buna göre,
• 32’şer gram karbon ( C ) ve oksijen ( O ) elementlerinin tam verimli tepkimesinden 44 gram CO2 bileşiği oluşurken 20 gram karbon elementi artıyor.
• 56 gram karbon monoksit ( CO ) bileşiği tamamen analiz edildiğinde 32 gram oksijen elementi ile 24 gram karbon elementi elde ediliyor.
deneylerini yapan bir öğrenci;
I. kütlenin korunumu,
II. katlı oranlar,
III. sabit oranlar
kanunlarından hangilerini ispatlayabilir?
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 6 |
Bir maddenin mol sayısı; ![]() formülleri kullanılarak hesaplanabilir.
formülleri kullanılarak hesaplanabilir.
Bazı maddelerin miktarları, kütle veya tanecik sayısı olarak tabloda verilmiştir.

Buna göre miktarı 0,2 mol olan maddelerin bulunduğu kutucukların taranmış hâli aşağıdakilerden hangisidir?
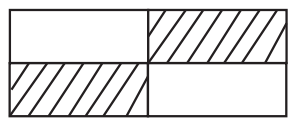 | |
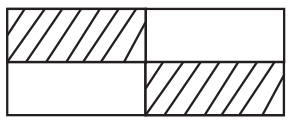 | |
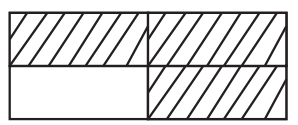 | |
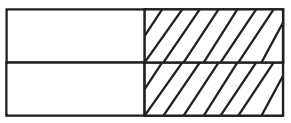 | |
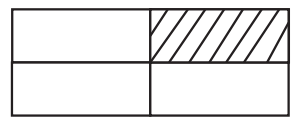 |
Soru 7 |
Mol kütlesi, maddelerin bir molünün kütlesidir. Bileşiklerin mol kütlesi hesaplanırken, bileşiğin yapısında yer alan elementlerin mol sayıları ile atom kütleleri ayrı ayrı çarpılıp toplanır. Örneğin atom kütleleri sırasıyla 12 g, 1 g ve 16 g olan C,H ve O elementlerinden oluşan C2H6O bileşiğinin mol kütlesi:
(12.2) + (6.1) + (16.1) = 46 g şeklinde hesaplanır. Bu işlem sonucunda, “1 mol C2H6O bileşiği 46 gramdır” ifadesine ulaşılır.
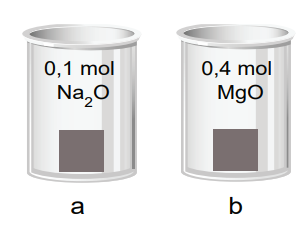
Buna göre yukarıda verilen a ve b kaplarında eşit kütlelerde madde bulunmasını isteyen Ömer,
I. a kabına 0,1 mol Fe2O3 ile 0,3 mol H2O, b kabına 0,2 mol NaCl eklemelidr.
II a kabına 0,3 mol H2O ile 0,2 mol NaCl, b kabına 0,1 mol Fe2O3 eklemelidir.
III. a kabına 0,2 mol Fe2O3, b kabına 0,1 mol H2O ile 0,3 mol NaCl eklemelidir.
işlemlerinden hangilerini ayrı ayrı yapabilir?
( H:1 g/mol, O:16 g/mol, Na:23 g/mol, Mg:24 g/mol, Cl:35 g/mol, Fe:56 g/mol )
Yalnız I. | |
Yalnız II. | |
Yalnız III. | |
I ve II. | |
II ve III. |
Soru 8 |
0ºC sıcaklık ve 1 atmosfer basınç koşullarına normal koşullar denir. Normal koşullarda 1 mol gaz 22,4 litre hacim kaplar.
Tabloda L, M ve T maddelerinin 1 atmosfer basınçtaki hâl değişim sıcaklıkları verilmiştir.
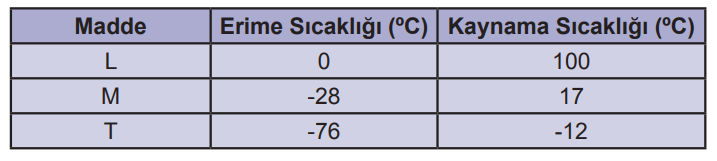
Tabloya göre aşağıdaki ifadelerden hangisi doğrudur?
0,1 mol L maddesinin normal koşullardaki hacmi 2,24 litredir. | |
Normal koşullarda 11,2 litre hacim kaplayan M maddesi 0,5 moldür. | |
0,3 mol T maddesinin normal koşullardaki hacmi 6,72 litredir. | |
0,2 mol L maddesinin normal koşullardaki hacmi 4,48 litredir. | |
Normal koşullarda 44,8 litre hacim kaplayan M maddesi 2 moldür. |
Soru 9 |
Bor elementinin en kararlı izotopları ![]() Bu izotopların doğada bulunma yüzdeleri sırasıyla %20 ve %80 olup bor elementinin ortalama atom kütlesi 10,8’dir.
Bu izotopların doğada bulunma yüzdeleri sırasıyla %20 ve %80 olup bor elementinin ortalama atom kütlesi 10,8’dir.
Ülkemizde 10B izotop oranı yüksek bor cevher yatakları bulunmaktadır.
10B nin 5 nötronu, 11B nin 6 nötronu vardır. 5 nötronu olan 1 nötron almaya çalışırsa patlayabilir ve çok yüksek enerjili partiküller yayar. Bu enerji herhangi bir hücreyi öldürebilecek güçtedir.
10B elementi kanser hücresine girerse kanser hücresini, sağlıklı hücreye girerse sağlıklı hücreyi öldürür. Bilim insanlarının görevi 10B elementini kanser hücresine yönlendirmek olmalıdır.
Bu metne göre,
I. Proton sayıları aynı, nötron sayıları farklı olan atomlar izotop atomlardır.
II. İzotop atomların doğada bulunma yüzdelerinden ortalama atom kütlesi hesaplanabilir.
III. 10B elementi ile kanser hastalığı tedavi edilebilir.
yargılarından hangilerine ulaşılabilir?
Yalnız I. | |
Yalnız II. | |
I ve II. | |
II ve III. | |
I, II ve III. |
Soru 10 |
Doğadaki birçok olay kimyasal değişimler sonucu gerçekleşir. Kimyasal tepkime bir veya daha fazla maddenin yeni maddelere dönüşmesidir. Kimyasal tepkimeler kimyasal denklemlerle ifade edilir. Yanıcı maddenin oksijenle tepkimeye girmesine yanma, tepkimeye ise yanma tepkimesi denir. İki veya daha fazla kimyasal türün tepkimeye girerek bileşik oluşturmasına sentez (oluşum) tepkimesi denir. Bir bileşiğin ısı veya elektrik enerjisiyle daha küçük kimyasal türlere ayrışması analiz (ayrışma) tepkimesi şeklinde tanımlanır.
Buna göre aşağıdaki tepkimelerden hangisi verilen tanımlara uymaz?
HCl(suda) + NaOH(suda) → NaCl(k) + H2 O(s) | |
N2 (g) + 3H2 (g) → 2NH3 (g) | |
CaCO3 (k) → CaO(k) + CO2 (g) | |
CH4 (g) + 2O2 (g) → CO2 (g) + H2 O(g) | |
C(k) + O2 (g) → CO2 (g) |
10. Sınıf Kimya Tarama Testi PDF Test
10. Sınıf Kimya Tarama Testi konusuyla ilgili sorular bulunmaktadır. Testler; kazanım odaklı güncel sorulardan oluşmaktadır.
Test İstatistikleri (Ortalama)
| Doğru | 6.00 |
| Yanlış | 3.50 |
| Net | 4.84 |
| Çözülme Sayısı | 2 |
Başarı Tablosu
| İsim Soyisim | Doğru | Yanlış | Süre |