Soru 1 |
2Mg(k) + O2 (g) → 2MgO(k) tepkimesi resimde görülen havai fişeklerde beyaz kıvılcımlar oluşturmak için kullanılır. Çünkü Mg metali parlak beyaz ışık vererek yanar.

Tepkime devam ederken katı Mg parçasındaki Mg atomları elektron vererek Mg2+ iyonlarını oluştururken moleküler oksijendeki O atomları elektron alarak O2- iyonlarını oluşturur.
Buna göre,
I. Magnezyum atomları yükseltgendir.
II. Oksijen atomları indirgenmiştir.
III. Havai fişeklerdeki beyaz kıvılcım oluşumu redoks olayıdır.
ifadelerinden hangileri doğrudur?
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 2 |
Bir atom ya da iyonun elektron almasıyla gerçekleşen olaya indirgenme, elektron vermesiyle gerçekleşen olaya yükseltgenme denir.
• E0pil > 0 ise tepkime istemlidir.
• E0pil < 0 ise tepkime istemsizdir.
• Pil potansiyeli büyüdükçe tepkimenin istemliliği artar.
Buna göre,
I. Zn(k) +2Ag+(suda) ![]() Zn2+(suda) +2Ag(k) E0pil= 1,562 V
Zn2+(suda) +2Ag(k) E0pil= 1,562 V
II. Cu(k) +Mg2+(suda) ![]() Cu2+(suda) +Mg(k) E0pil= -2,709 V
Cu2+(suda) +Mg(k) E0pil= -2,709 V
III. 2Al(k) +3Cu2+(suda) ![]() 2Al3+(suda) +3Cu(k) E0pil= 1,999 V
2Al3+(suda) +3Cu(k) E0pil= 1,999 V
tepkimeleri ile ilgili aşağıdaki ifadelerden hangisi yanlıştır?
I. tepkimede Zn atomları yükseltgenmiştir. | |
II. tepkime, III. tepkimeye göre daha istemlidir. | |
I. tepkime yazılan yönde istemlidir. | |
III. tepkime, I. tepkimeye göre daha istemlidir. | |
II. tepkime yazılan yönde istemsizdir. |
Soru 3 |
Elektrokimyasal pil devrelerinde iki tane yarı hücre bulunur. Yarı hücrelerin içinde elektrolit çözeltiler ve bu çözeltilere batırılmış elektrot adı verilen metal çubuklar bulunur. Elektrotlar dış devrede iletken bir tel ile birbirine bağlanır. Aktif metalden yapılmış elektrot, elektron verip çözünürken pasif olan elektrodun bulunduğu yarı hücredeki elektrolit çözeltinin katyonu elektron alarak indirgenir. Böylece iletken telde elektron akışı sağlanır ve kimyasal enerji elektrik enerjisine dönüşür.

Evlerde kullandığımız birçok maddeden elektrik enerjisi elde edebiliriz. Örneğin limona bakır ve çinko levhalar batırılıp iletken tel ile birbirlerine bağlanarak basit bir pil devresi kurulmuş olur.
Çinkonun aktifliği bakırdan büyük olduğuna göre limon pili düzeneği ile ilgili,
I. Çinko ile bakır levha arasındaki iletken telde elektronlar çinkodan bakıra doğru geçer.
II. Limon suyundaki katyonlar çinkonun etrafında indirgenirler.
III. Zamanla bakır levhanın kütlesi azalır.
ifadelerinden hangileri doğrudur?
Yalnız I. | |
Yalnız II. | |
Yalnız III. | |
I ve II. | |
II ve III. |
Soru 4 |
Metallerin aktiflik sıralamasına göre çözeltilerin hangi kaplarda saklanacağı belirlenir. Metal kaplara konulacak çözeltideki metal iyonunun aktifliği kabın yapıldığı metalin aktifliğinden daha fazla olmalıdır. Aksi durumda kap ile çözelti arasında tepkime gerçekleşecek ve kap aşınacaktır.
Buna göre aktiflikleri Ni > Cu > Ag şeklinde sıralanan,
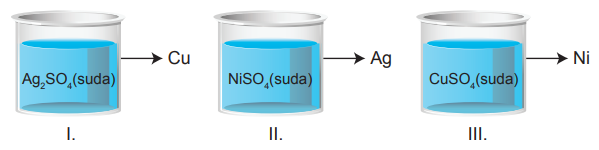
kaplarından hangilerinde içindeki çözelti saklanamaz?
Yalnız I. | |
Yalnız II. | |
I ve II. | |
I ve III. | |
I, II ve III. |
Soru 5 |
Kimyasal piller indirgenme-yükseltgenme tepkimeleri üzerinden yürüyen elektron hareketi ile çalışır. İki ayrı yarı hücrede bulunan elektrolit çözeltilere batırılmış, genellikle metal malzemelerden yapılan çubuklar elektrot olarak adlandırılırlar. Standart indirgenme potansiyeli küçük olan elektrot anot, diğer elektrot katottur. Anot elektrot yükseltgenerek çözeltiye geçer ve dış devreye elektron verir, katot elektrodun bulunduğu yarı hücre içindeki çözeltide bulunan katyonlardan biri anottan gelen elektronu alarak indirgenir. Elektrolit çözeltilerde değişen katyon derişimlerini dengelemek için tuz köprüsü pil devresinde bulunmak zorundadır. Tuz köprüsünün içinde genellikle NaCl veya KCl sulu çözeltileri bulunur. Tuz köprüsündeki anyonlar anot yarı hücresine, katyonlar katot yarı hücresine geçerler.
Şekilde bir elektrokimyasal pil düzeneği gösterilmiş ve bu pilin yarı tepkimelerinin indirgenme potansiyelleri verilmiştir.
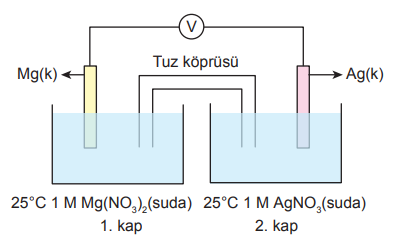
Mg2+(suda) + 2e- → Mg(k) Eo = -2,37 V
Ag+(suda) + e- → Ag(k) Eo = +0,80 V
Buna göre aşağıdaki ifadelerden hangisi yanlıştır?
Tuz köprüsündeki anyonlar, Ag elektrodun bulunduğu yarı hücreye, katyonlar ise Mg elektrodun bulunduğu yarı hücreye doğru geçer. | |
Mg elektrot anot, Ag elektrot katottur. | |
Mg elektrodun bulunduğu yarı hücrede zamanla Mg2+ derişimi artarken Ag elektrodun bulunduğu yarı hücrede zamanla Ag+ derişimi azalır. | |
Dış devrede elektron hareketi, Mg elektrodun bulunduğu yarı hücreden Ag elektrodun bulunduğu yarı hücreye doğrudur. | |
Zamanla Mg elektrodun kütlesi azalırken, Ag elektrodun kütlesi artar. |
Soru 6 |
• Standart indirgenme potansiyeli küçüldükçe metalin aktifliği artar.
• Metal atomu çözeltideki metal iyonundan daha aktif ise metal aşınır.
Aşağıda bazı iyonların indirgenme yarı tepkimeleri ve standart indirgenme potansiyelleri verilmiştir.
X2+(suda) + 2e- → X(k) Eo = -0,76 V
Y2+(suda) + 2e- → Y(k) Eo = -0,25 V
Z2+(suda) + 2e- → Z(k) Eo = +0,34 V
Buna göre,
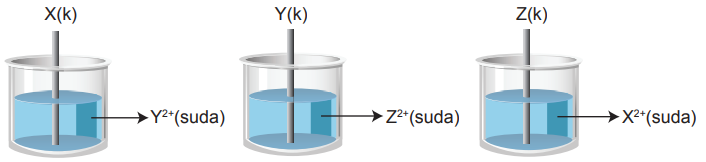
X, Y ve Z metal çubuklarından hangilerinde aşınma gerçekleşir?
X, Y ve Z metal çubuklarından hangilerinde aşınma gerçekleşir? | |
Yalnız Z | |
X ve Y | |
Y ve Z | |
X, Y ve Z |
Soru 7 |
Metal aktiflik, metallerin elektron verme eğiliminin bir ölçüsüdür. Aktif bir metal, kendisinden pasif ve bileşik oluşturmuş bir metalin yerine kendiliğinden geçer. Bu sırada aktif metal yükseltgenir, pasif metal indirgenir.
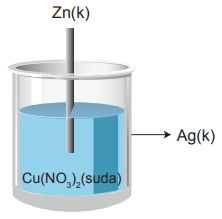
Şekilde Ag metalinden yapılmış kabın içinde Cu(NO3)2 sulu çözeltisi bulunmaktadır. Çözeltiye Zn metalinden yapılmış bir çubuk batırıldığında Zn çubuğun üzerinin Cu metali ile kaplandığı gözleniyor. Bu sırada Ag metalinden yapılmış kapta bir aşınma olmadığı görülüyor.
Buna göre,
I. Çözeltide Zn2+ iyonlarının derişimi artar.
II. Ag metalinin elektron verme eğilimi Cu ve Zn metallerinin elektron verme eğiliminden düşüktür.
III. Cu metalinden yapılmış kapta Zn(NO3)2 çözeltisi saklanabilir.
yargılarından hangileri doğrudur?
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 8 |
• Elektrokimyasal pilin potansiyeli sıcaklıkla ters orantılıdır.
• Elektrokimyasal pillerde gerçekleşen tepkimeler denge tepkimesi olduğundan, dış etkilere karşı Le Chatelier İlkesi’ne göre dengeye ulaşma eğilimi gösterir. Yani dışarıdan yapılan etki sonucunda artırılan bir niceliği azaltacak şekilde, azaltılan bir niceliği de artıracak şekilde değişim gösterir.
Şekilde bir elektrokimyasal pil düzeneği gösterilmiştir.
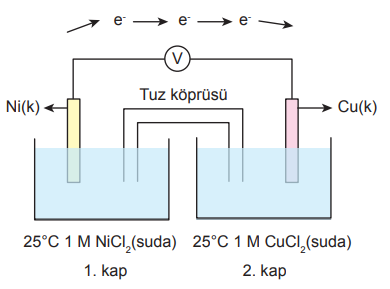
Buna göre aşağıdaki ifadelerden hangisi yanlıştır?
Pil tepkimesi Ni(k) + Cu2+(suda) | |
1. kaba saf su ilave edilirse pil potansiyeli artar. | |
Sıcaklık arttırıldığında pil potansiyeli azalır. | |
1. kaba bir miktar K2S katısı ilave edilirse pil potansiyeli artar. (NiS suda az çözünür.) | |
2. kaba bir miktar CuCI2 katısı ilave edilirse pil potansiyeli azalır. |
Soru 9 |
Alman bilim insanı Nerst 25°C’ta standart pil potansiyeli (E0 pil) ile derişimi 1 M den farklı olan pil potansiyeli (Epil) arasındaki ilişkiyi araştırmış ve ![]() eşitliğini bulmuştur. Bu eşitliğe Nerst eşitliği denir.
eşitliğini bulmuştur. Bu eşitliğe Nerst eşitliği denir.
25°C’ta pil tepkimesi,
Zn(k) + Cu2+ (0,01 M) ![]() Zn2+ (0,0001 M) + Cu(k) E0 pil =1,1 V
Zn2+ (0,0001 M) + Cu(k) E0 pil =1,1 V
şeklinde olan pil ile ilgili,
I. Zn yarı hücresinde yükseltgenme olmuştur.
II. Zamanla Cu2+ iyonlarını içeren çözeltinin derişimi azalır.
III. Derişimdeki değişim pil potansiyelinin azalmasına sebep olmuştur.
ifadelerinden hangileri doğrudur?
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 10 |
Şekilde bir elektrokimyasal pil düzeneği gösterilmiştir.
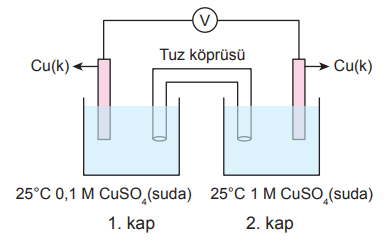
Buna göre aşağıdakilerden hangisi yanlıştır?
( Nernst sabiti = 0,0592 )
2. kaba saf su eklenirse pil potansiyeli artar. | |
Zamanla tuz köprüsündeki anyonlar 1. kaba geçer. | |
Epil = 0,0296 V’tur. | |
Zamanla 2. kabın derişimi azalır. | |
1. ve 2. kaplardaki çözeltilerin derişimleri eşitlenince pil çalışmaz. |
12. Sınıf Kimya Korozyon PDF Test
12. Sınıf Kimya Korozyon konusuyla ilgili sorular bulunmaktadır. Testler; kazanım odaklı güncel sorulardan oluşmaktadır.
Test İstatistikleri (Ortalama)
| Doğru | 2 |
| Yanlış | 8 |
| Net | -0.67 |
| Çözülme Sayısı | 1 |
Başarı Tablosu
| İsim Soyisim | Doğru | Yanlış | Süre |
| Zilan ince | 2 | 8 | 29 saniye |